Een experimentele behandeling met bacteriebestrijdende virussen heeft volgens een nieuw rapport mogelijk bijgedragen aan het redden van het leven van een Britse tiener met een kritieke 'superbug'-infectie.
De tiener, de 17-jarige Isabelle Carnell-Holdaway, heeft cystische fibrose en ontwikkelde een wijdverbreide bacteriële infectie na een longtransplantatie om haar aandoening in 2017 te behandelen. (Cystische fibrose is een genetische aandoening die resulteert in schade aan het ademhalingssysteem en andere organen, en verhoogt het risico op longinfecties.) Ondanks behandeling met antibiotica, verspreidden de bacteriën zich naar haar operatiewond, haar lever en meer dan 20 andere locaties op haar huid. Haar prognose was grimmig - één arts gaf haar minder dan 1% overlevingskans, volgens CNN.
Maar dat veranderde allemaal nadat ze werd behandeld met een cocktail van drie virussen die specifiek aanvallen Mycobacterium abscessus, de gevaarlijke bacterie die haar infectie veroorzaakt. Twee van de drie virussen werden genetisch aangepast om ze te helpen de bacteriën beter te doden, wat de eerste keer is dat Isabelle genetisch gemodificeerde virussen gebruikt om antibiotica-resistente infecties te behandelen, aldus de auteurs.
Na haar behandeling begon de toestand van Isabelle te verbeteren: haar chirurgische wond genas geleidelijk, net als andere delen van de geïnfecteerde huid, volgens het rapport dat op 8 mei in het tijdschrift Nature Medicine werd gepubliceerd. Ze begon aan te komen en is teruggekeerd naar school, meldde CNN.
Maar hoe werkt deze therapie?
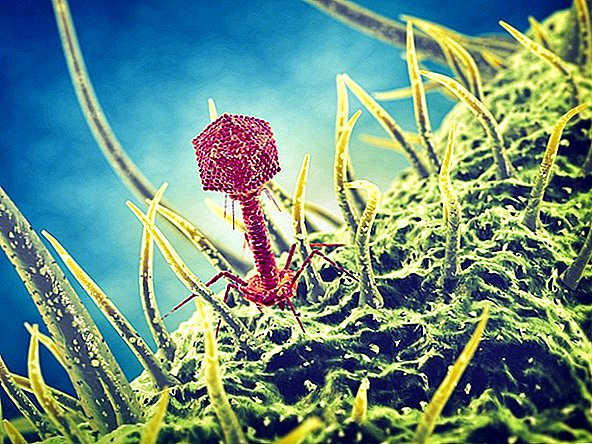
De behandeling maakt gebruik van speciale soorten virussen die bekend staan als "bacteriofagen" of kortweg fagen, die alomtegenwoordig zijn op de planeet. Deze virussen hebben één specialiteit: ze infecteren van nature bacteriën. Zodra ze dat doen, repliceren de virussen in de bacteriële cel en doden ze door dit replicatieve proces de bacterie, zei co-auteur Graham Hatfull, een professor in biologische wetenschappen aan de Universiteit van Pittsburgh.
Een tweesnijdend zwaard"
Maar als deze bacteriedodende virussen zo effectief zijn, waarom is hun gebruik dan niet meer wijdverspreid?
In feite zijn fagen zeer specifiek voor de bacteriën die ze infecteren - wat betekent dat een bepaalde faag slechts één bacteriestam kan infecteren - wat een "beetje een tweesnijdend zwaard is", vertelde Hatfull aan WordsSideKick.com. Aan de ene kant werken de virussen als "geleide raketten die de specifieke pathogenen waarmee een patiënt is geïnfecteerd achterna gaan, en de rest van het microbioom en alle andere bacteriën met rust laten", zei Hatfull. Dat betekent dat faagtherapie meestal geen bijwerkingen heeft. Maar aan de andere kant kunnen ze zo specifiek zijn dat een faag die voor één patiënt met een bepaalde infectie werkt, mogelijk niet werkt voor een andere patiënt die besmet is met dezelfde soort bacteriën, zei hij.
In het geval van Isabelle kamden onderzoekers door een verzameling van ongeveer 10.000 fagen - samengesteld door het laboratorium van Hatfull - voor degenen die zouden werken tegen de bacteriële stam waarmee ze besmet was. Dit omvatte het doorzoeken van de 10.000 fagen om ze te beperken tot ongeveer 50 tot 100 van de beste kandidaten, en deze kandidaten afzonderlijk te screenen op hun vermogen om te infecteren M. abscessus, Zei Hatfull.
Uiteindelijk vonden de onderzoekers slechts één faagvirus dat de bacteriën effectief kon infecteren en doden. Ze hebben twee andere gevonden die kunnen infecteren M. abscessus, maar waren niet erg goed in het doden van de bacteriën. Dus de onderzoekers hebben deze twee virussen genetisch gemodificeerd om ze te veranderen van 'arme moordenaars in ... echt goede moordenaars', zei Hatfull.
Opnieuw opduiken om een groeiende dreiging te bestrijden
Het idee om fagen te gebruiken om bacteriële infecties te behandelen bestaat al ongeveer 100 jaar, maar werd grotendeels vergeten met de ontdekking van antibiotica. Pas in de afgelopen decennia is de belangstelling voor het gebied opnieuw opgekomen vanwege de toenemende dreiging van antibioticaresistentie.
Het is belangrijk op te merken dat Isabelle nog steeds niet volledig genezen is van haar infectie. En omdat bij deze studie slechts één patiënt betrokken was, kunnen de onderzoekers niet met zekerheid zeggen of het herstel van Isabelle rechtstreeks het gevolg was van de faagtherapie (hoewel het bewijs suggereert dat dit wel het geval was).
De onderzoekers zeiden dat ze hopen dat het nieuwe werk meer studies op dit gebied aanmoedigt.
De nieuwe casus laat zien dat "wanneer we een goede set fagen matchen met een bepaalde infectie bij een patiënt, we de infectie effectief kunnen beheersen ... en we deze patiënt kunnen redden", zei Hatfull.
Toekomstige studies zouden vragen moeten onderzoeken, zoals welke ziekten het best kunnen worden behandeld met faagtherapie, welke dosis nodig is en hoe lang de therapie zou worden toegediend, zei Hatfull.
Het nieuwe werk is slechts een kleine stap in het grote geheel van faagtherapie, maar een 'enorme stap voor de patiënt', zei Hatfull.